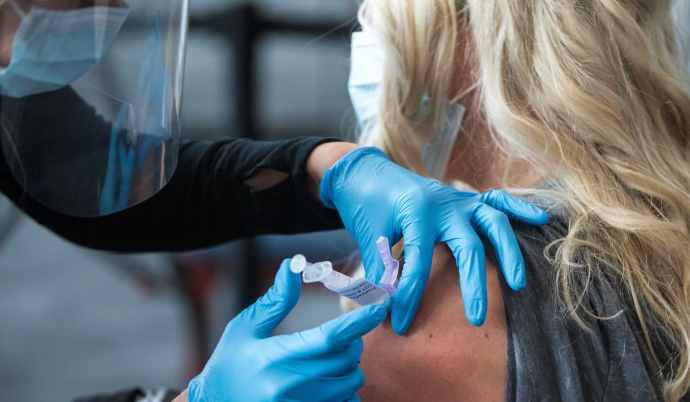
Emily Hood aveva già battuto le probabilità. All’età di 17 anni, le era stato diagnosticato un tumore estremamente raro e inoperabile in agguato nella parte inferiore del suo cervello. Un anno e mezzo dopo era ancora viva, il che la collocava in una minoranza molto fortunata. Le persone con la sua forma di cancro al cervello, noto come glioma pontino intrinseco diffuso (DIPG), generalmente sopravvivono solo per 8-11 mesi dopo la diagnosi. A 18 anni, Emily, in un ultimo disperato tentativo di combattere il cancro, ha deciso di offrirsi volontaria per una terapia cellulare sperimentale che sfrutta il potere del sistema immunitario:
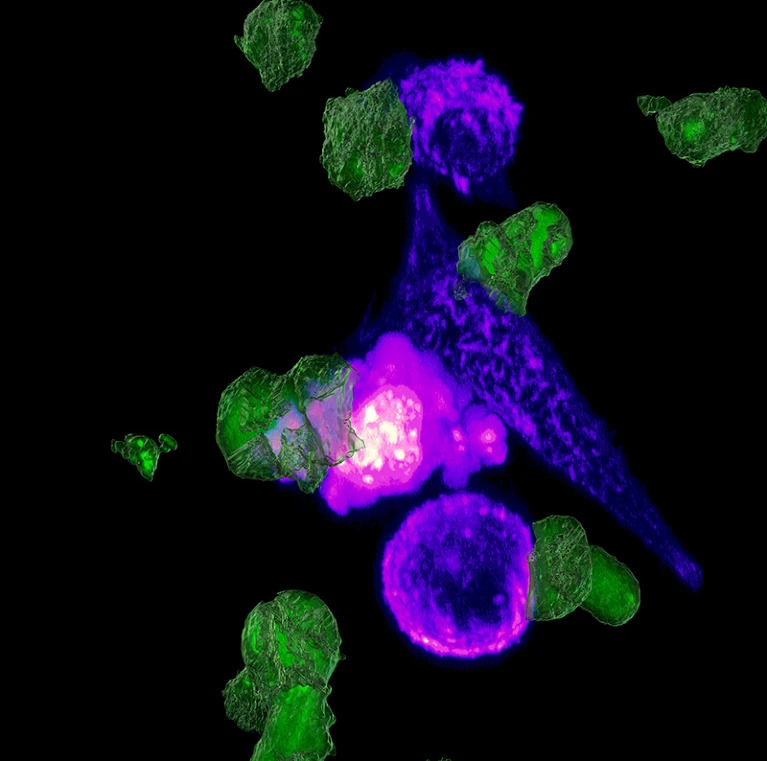
Gli scienziati del Seattle Children’s Hospital di Washington hanno raccolto cellule immunitarie – chiamate cellule T – dal sangue di Emily e le hanno dotate di una proteina di superficie nota come recettore chimerico dell’antigene (CAR). Questa proteina si lega a un bersaglio specifico sulle cellule tumorali, creando cellule T che combattono il tumore che possono insediarsi e uccidere il tessuto canceroso. Nell’ottobre 2020, i medici hanno iniettato le cellule geneticamente riprogrammate attraverso una porta impiantata sotto il cuoio capelluto di Emily. È stata la prima persona con DIPG al mondo a ricevere la terapia con cellule CAR-T somministrata direttamente nel cervello.
Le cellule CAR-T hanno rivoluzionato il trattamento di alcuni tumori del sangue, tra cui una forma pediatrica di leucemia che rappresenta circa un quarto di tutte le neoplasie infantili. Ma finora l’immunoterapia cellulare non è riuscita a ridurre il carico di tumori solidi, come quello che si stava diffondendo nel tronco encefalico di Emily. E, sebbene vi sia un’immensa necessità clinica di estendere le terapie con cellule CAR-T a tutti i regni dell’oncologia dei tumori solidi, indipendentemente dall’età della persona, i medici che trattano i tumori infantili di organi come il cervello, le ossa e i muscoli affermano che il bisogno è particolarmente acuto nei minori di 18 anni.
Un’occasione per crescere
“In oncologia pediatrica, non c’è molta alternativa”, afferma Claudia Rössig, immunoterapista cellulare presso l’ospedale universitario di Münster in Germania. Per i tumori degli adulti esistono agenti mirati e farmaci immunomodulanti che possono prolungare la vita delle persone, spesso per molti anni. Ma per i bambini, questi tipi di terapie all’avanguardia sono in gran parte falliti. Inoltre, osserva Rössig:

“In ambito pediatrico, non ci basta guadagnare tempo. Dobbiamo curare [il cancro]”, dice, “e poiché le cellule T hanno questa proprietà endogena di essere in grado di persistere, rimanere indietro e controllare la malattia per lungo tempo, hanno la capacità di essere curative“. Stando a quanto si apprende, tale tecnica è già stata utilizzata in precedenza per contrastare la leucemia pediatrica. I tumori solidi potrebbero essere i prossimi. Come ricorda sua madre Sharon Hood, Emily era in parte motivata dalla ricerca di far progredire il progresso medico verso nuove cure per la malattia. “Lo faceva sempre non solo per se stessa, ma in modo che, si spera, i bambini piccoli [con DIPG] avessero la possibilità di crescere.” Emily non riuscirà a vederlo accadere. Ma i medici che hanno condotto prove di terapie con cellule CAR-T in persone come Emily sono più ottimisti che mai sul fatto che un giorno del genere arriverà.
“Ci sono diversi pazienti – una frazione considerevole – che stanno riscontrando benefici”, afferma Crystal Mackall, ricercatrice di immunoterapia del cancro presso la Stanford University School of Medicine in California. Insieme ai suoi colleghi, Mackall ha curato circa una dozzina di bambini con DIPG con un diverso prodotto CAR-T-cell. I ricercatori hanno persino osservato un’eliminazione quasi completa del cancro al cervello in un ricevente adolescente. “Non è un fuoricampo“, dice Mackall. Ma è un’indicazione del potenziale del trattamento che, come sottolinea Nicholas Vitanza, un neuro-oncologo del Seattle Children’s Hospital che ha curato Emily, “è ciò che ci spinge a migliorare la prossima generazione di cellule CAR-T”.
I miglioramenti stanno arrivando da una serie di direzioni diverse. I ricercatori stanno scoprendo nuovi bersagli che potrebbero portare a terapie più sicure ed efficaci. Stanno incorporando circuiti genetici aggiuntivi per aiutare le cellule a persistere più a lungo e rimanere attive nel corpo. E stanno trovando modi per sovvertire la capacità dei tumori di sopprimere le risposte immunitarie. Molte di queste innovazioni saranno necessarie per mantenere l’immensa promessa delle cellule CAR-T per i tumori solidi sia negli adulti che nei bambini. Ma la biologia dei tumori pediatrici, che per lo più derivano da irregolarità nelle prime fasi di sviluppo cellulare, è fondamentalmente diversa da quella dei tumori degli adulti, che insorgono tipicamente attraverso una vita di mutazioni acquisite. E dati questi distinti meccanismi della malattia, dicono i ricercatori, è necessario uno sforzo di scoperta dedicato per adattare la progettazione delle cellule CAR-T ai tumori infantili.
Il tipico approccio a cascata di riproporre le terapie che sono state sviluppate per i tumori degli adulti semplicemente non funzionerà, affermano i ricercatori. E con poche opzioni terapeutiche disponibili per il 20% dei bambini i cui tumori non possono essere contenuti solo con chemioterapia, chirurgia e radiazioni, c’è un urgente bisogno di nuovi approcci terapeutici che possano ripulire il cancro. Le cellule CAR-T, se costruite nel modo giusto, offrono quel tipo di potenziale di trattamento, il che spiega perché si stanno facendo così tanti sforzi per far funzionare la piattaforma per i bambini. “La nostra visione è di rendere le terapie con cellule T standard di cura per i tumori solidi pediatrici entro un decennio”, afferma Catherine Bollard, terapista cellulare pediatrico presso il Children’s National Hospital di Washington DC. “È davvero audace”, ammette, ma anche, sostiene, un obiettivo raggiungibile.
Allenamento di tiro al bersaglio
Finora, la maggior parte degli studi clinici che coinvolgono le cellule CAR-T per i tumori solidi pediatrici si sono concentrati su un numero selezionato di bersagli, principalmente proteine come B7-H3 (noto anche come CD276) o molecole complesse di zucchero-grasso, come GD2, che sono comunemente espresso ad alti livelli sulla superficie delle cellule tumorali infantili ma raramente espresso nei tessuti normali. “Quindi, con un prodotto a base di cellule CAR-T possiamo trattare pazienti con molte malattie diverse”, afferma Christopher DeRenzo, oncologo pediatrico presso il St. Jude Children’s Research Hospital di Memphis, nel Tennessee, che sta attualmente conducendo uno studio per le persone sotto la 21 anni con qualsiasi cancro che esprime B7-H3.
Questo è importante, afferma Katie Albert, oncologa del Seattle Children, perché anche i tumori solidi più comuni sono estremamente rari nei bambini: ogni tumore colpisce in genere solo poche centinaia di giovani all’anno negli Stati Uniti. Questa scarsità rende difficile sviluppare terapie ed eseguire sperimentazioni per un singolo tipo di cancro. Ma diventa fattibile quando quei tumori rari condividono un antigene comune. Come spiega Albert: “L’obiettivo è scegliere obiettivi con il maggiore impatto”. Tuttavia, gli obiettivi perseguiti sono tutt’altro che ideali. Molti degli antigeni non sono universalmente espressi su tutte le cellule di un tumore e basta un piccolo gruppo di cellule evasive per seminare una ricaduta. Inoltre, poiché le molecole bersaglio non sono essenziali per la sopravvivenza cellulare, i tumori possono sviluppare modi per abbandonarle per diventare resistenti alle immunoterapie cellulari.
“Non esiste un obiettivo perfetto“, afferma Rössig. Forse non sorprende quindi che solo un’infarinatura di bambini abbia visto i propri tumori solidi ridursi drasticamente dopo la terapia con cellule CAR-T. Vitanza, ad esempio, ha condotto prove su tre prodotti a base di cellule CAR-T antigene e ha somministrato centinaia di infusioni di cellule a più di 60 bambini. E sebbene il tumore di un bambino affetto da DIPG sia stato sconfitto con successo per più di 14 mesi e, con infusioni ogni 2 settimane, non abbia segni di crescita, le risposte della maggior parte dei bambini sono state molto più attenuate 1 . Ciò fa eco alle scoperte di altri. Nel Regno Unito 2 e in Cina 3 , ad esempio, i ricercatori hanno valutato le cellule CAR-T anti-GD2 in piccole coorti di persone con neuroblastoma recidivato, un tumore pediatrico del tessuto nervoso. Le terapie hanno superato i test di sicurezza, ma nessun bambino ha sperimentato una riduzione del tumore in nessuno dei due studi.
Con la fattibilità ora stabilita, un modo per migliorare questi primi costrutti di cellule CAR-T è con nuovi bersagli che rappresentano meglio le peculiarità di vari tumori infantili – e a guidare la ricerca di nuovi antigeni tumorali è Misty Jenkins, immunologa del cancro presso il Walter e l’Eliza Hall Institute of Medical Research di Melbourne, in Australia. Concentrandosi sui tumori cerebrali pediatrici, Jenkins ei suoi colleghi hanno sistematicamente caratterizzato le proteine trovate sulla superficie dei tessuti sottoposti a biopsia. Nel lavoro non pubblicato, dice, “abbiamo identificato una serie di nuovi bersagli”, inclusi molti che, sebbene non mutati geneticamente, sono alterati in modi che potrebbero consentire loro di essere mirati in modo selettivo.
I ricercatori del Children’s Hospital of Philadelphia (CHOP) in Pennsylvania hanno un altro approccio. Invece di cercare proteine adeguate della superficie cellulare, il team si è concentrato sulle proteine che normalmente si trovano solo all’interno della cellula, la cui presenza viene visualizzata sulla superficie attraverso un meccanismo di allerta immunitario specializzato. I ricercatori hanno dimostrato che le cellule CAR-T dirette contro uno di questi bersagli potrebbero eliminare il neuroblastoma nei modelli murini 4 . Stanno progettando di iniziare una sperimentazione clinica nel 2023.
Celle imbottite
Anche con la suite esistente di antigeni, risultati migliori potrebbero derivare dalla somministrazione di cellule CAR-T più potenti. Bollard pensa che questo potrebbe essere realizzabile, in parte, preselezionando le cellule immunitarie delle persone con cancro per le cellule T già preparate a rilevare i tumori, e quindi ingegnerizzando i costrutti CAR in quelle cellule preattivate. Ora, attraverso una sovvenzione quinquennale da 25 milioni di dollari assegnata nel giugno 2022, Bollard sta mettendo alla prova l’idea.
Insieme ai collaboratori dell’University College di Londra e di Stanford, Bollard prevede di condurre tre studi clinici paralleli sulle cellule CAR-T che mirano a B7-H3 per i tumori pediatrici. Due studi si concentreranno sui sarcomi dei tessuti molli, con una differenza fondamentale: uno utilizzerà cellule T non selezionate senza fase di pre-screening; l’altro dispiegherà le cellule T scelte per la loro capacità di riconoscere un antigene tumorale comune noto come PRAME. Un terzo studio utilizzerà cellule T non selezionate che, dopo l’ingegnerizzazione, vengono somministrate mediante iniezione diretta nel cervello di bambini con tumori ad alto rischio.
“Saremo in grado di fare un confronto diretto negli studi clinici sull’importanza della cellula T che stai progettando”, afferma Bollard. Oltre al costrutto CAR, le cellule T in tutti e tre questi studi riceveranno un’ulteriore modifica genetica: trasporteranno una proteina extra che elimina i fattori di crescita che normalmente bloccano la capacità delle cellule T di colpire il loro bersaglio. Inoltre, queste proteine che aspirano il fattore di crescita sono progettate per trasformare il segnale solitamente repressivo in uno che aumenta invece l’attività delle cellule T. “Sta trasformando un negativo in positivo”, dice Bollard.
Questa è solo una delle tante modifiche che i ricercatori stanno ora incorporando nei perfezionamenti della terapia con cellule CAR-T per trattare i tumori solidi nei bambini. Altri stanno aggiungendo molecole di segnalazione o recettori co-stimolatori che danno alle cellule T una spinta in più per proliferare. Alcuni stanno incorporando fattori che aiutano a prevenire che le cellule T vengano sovrastimolate e entrino in uno stato disfunzionale ed esausto. “Da un punto di vista ingegneristico, le possibilità sono numerose”, afferma Karin Straathof, oncologa pediatrica presso l’University College London Great Ormond Street Institute of Child Health.
Alla School of Medicine dell’Università del Colorado ad Aurora, l’oncologo pediatrico Michael Verneris e i suoi colleghi hanno migliorato la capacità delle cellule CAR-T di viaggiare verso il loro sito tumorale bersaglio. In uno studio sui sarcomi infantili 5 , i ricercatori hanno scoperto che, dopo il trattamento con radiazioni, le cellule tumorali iniziano a vomitare la molecola di segnalazione interleuchina-8. Questa molecola è nota per attrarre alcuni tipi di cellule immunitarie, ma non le cellule T – di solito, le cellule T non esprimono il recettore per l’interleuchina-8 sulla loro superficie.
Quindi, il team di Verneris ha ingegnerizzato quella funzione nelle sue cellule CAR-T. I ricercatori hanno dimostrato che queste cellule potenziate dai recettori erano più potenti killer del cancro nei topi rispetto alle normali cellule CAR-T. Secondo Verneris, la funzionalità aggiunta ha promosso il movimento delle cellule verso i tumori e, come bonus, ha innescato cambiamenti metabolici che hanno reso le cellule più attive una volta che hanno raggiunto il sito del tumore.
Tuttavia, anche le cellule meglio progettate possono ancora affrontare sfide difficili, a meno che i ricercatori non affrontino anche le condizioni immunosoppressive che circondano la maggior parte dei tumori. “Questa è una delle variabili davvero importanti che definiranno davvero il successo delle cellule CAR-T e di altre immunoterapie nei tumori solidi infantili”, afferma Paul Ekert, genetista del cancro presso il Children’s Cancer Institute of Australia a Kensington. “Ma presuppone che conosciamo tutti i meccanismi che escludono le cellule T dai tumori infantili ad alto rischio”, aggiunge, “ed è qui che penso che abbiamo molto da imparare”.
Un indizio sulle sfide che le cellule CAR-T potrebbero affrontare nell’affrontare i tumori dei bambini è emerso all’inizio di quest’anno, quando i ricercatori hanno dimostrato nei topi portatori di cancro che l’ambiente tumorale nei cuccioli è particolarmente ostile all’infiltrazione delle cellule T 6 . Sebbene i ricercatori non abbiano studiato le cellule modificate con CAR, hanno scoperto che le cellule T non ingegnerizzate venivano spente più rapidamente nei topi giovani che negli animali più anziani. Tali differenze associate all’età nel microambiente tumorale potrebbero ostacolare gli sforzi per sviluppare cellule CAR-T efficaci per i tumori pediatrici.
#tumore #cancro #cervello #terapia
Fonte: https://www.nature.com/articles/d41586-022-04344-6