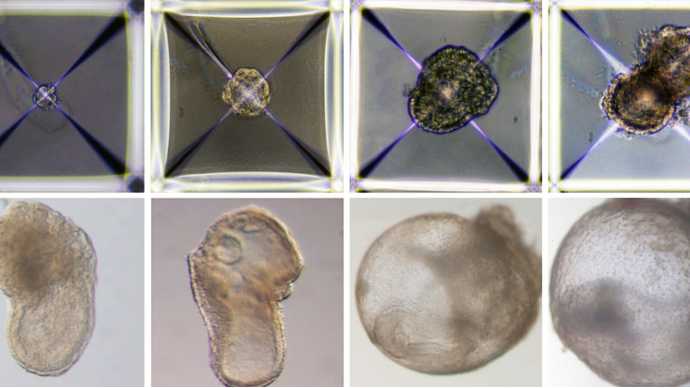
Al microscopio, gli embrioni di topo “sintetici” sembrano praticamente uguali a quelli concepiti in maniera naturale:
Come riportato dal gruppo di ricercatori responsabile degli esperimenti, condotti presso il Weizmann Institute of Science in Israele e pubblicati su Cell, infatti, gli embrioni il giorno 3 hanno cominciato ad allungarsi, da sfere a cilindri. Da un lato, il tubo neurale ha iniziato a piegarsi intorno al giorno 6, dall’altro ha iniziato a germogliare una coda. Entro il giorno 8, un cuore pulsante ha iniziato a far circolare il sangue attraverso i vasi che si formano attorno al sacco vitellino dell’embrione. Il tutto si è verificato senza l’uso di ovuli e senza sperma. Questi embrioni – confermano gli scienziati – non sono nemmeno cresciuti nell’utero di una femmina di topo:

Sono stati sviluppati all’interno di un bioreattore e costituiti interamente da cellule staminali coltivate in una capsula di Petri. Lo studio – a tratti inquietante e senz’altro controverso – apre nuove strade per studiare come le cellule staminali formano vari organi nell’embrione in via di sviluppo e per comprendere meglio come determinate mutazioni guidano varie malattie dello sviluppo. Solleva anche profonde domande sul fatto che altri animali, inclusi gli esseri umani, potrebbero un giorno essere coltivati da cellule staminali in un laboratorio. “Non appena la scienza inizia a spostarsi in un luogo in cui è possibile passare da una popolazione di cellule staminali in una capsula di Petri fino allo sviluppo di un organo, il che suggerisce che un giorno sarà possibile arrivare fino alla creazione di un organismo vivente: è un periodo piuttosto selvaggio e straordinario“, ha affermato Paul Tesar, biologo dello sviluppo presso la Case Western Reserve University School of Medicine che non è stato coinvolto nello studio. Dagli anni ’80, i biologi dello sviluppo hanno smontato gli embrioni cellula per cellula per cercare di capire come alla fine diventino tutti i tessuti specializzati che consentono ai pesci di nuotare, ai topi di correre e agli umani di camminare e parlare. Nell’ultimo decennio circa, i ricercatori hanno imparato abbastanza sui segnali che inviano le cellule staminali lungo questi percorsi di differenziazione per essere in grado di rimontarli in cose che assomigliano a organi (organoidi), uova fecondate di recente (blastoidi) e persino embrioni (embrioni).
Ma queste palline di topo e cellule umane potevano essere coltivate solo in piatti e provette per un breve lasso di tempo prima che espellessero. Avevano bisogno di un grembo vivo per sostenere il loro ulteriore sviluppo, o meglio ancora, una sua approssimazione artificiale. Jacob Hanna, un biologo di cellule staminali embrionali presso il Weizmann, ha trascorso sette anni a progettare un sistema di tubi di fiale di vetro rotanti alloggiate in un’incubatrice per fare proprio questo. L’anno scorso, il suo team ha riferito su Nature che il loro utero meccanico potrebbe mantenere in vita gli embrioni di topo naturale per un massimo di 11 giorni. “Questo ha davvero dimostrato che gli embrioni di mammiferi possono crescere al di fuori dell’utero – non si tratta di modellare o inviare segnali all’embrione, ma piuttosto di fornire supporto nutrizionale”, ha detto Hanna a STAT in un’intervista. Il passo successivo è stato vedere cosa sarebbe successo se avessero messo cellule staminali, piuttosto che embrioni naturali, nel loro aggeggio. “Queste cellule possono creare un intero embrione? Questa era una grande domanda senza risposta per il campo”.
In quest’ultimo lavoro, il team ha combinato quel sistema con un nuovo cocktail di cellule staminali, alcune delle quali erano state persuase chimicamente a sovraesprimere i geni che attivavano lo sviluppo della placenta e del sacco vitellino, tessuti vitali per sostenere la crescita sana di embrioni. Gli embrioni sintetici sono stati in grado di crescere fino al giorno 8,5, sviluppando l’inizio di un cervello ben modellato, un tubo neurale e un tratto intestinale, oltre a un cuore pulsante. Le analisi dei modelli di espressione genica degli embrioni sintetici su diversi tessuti hanno mostrato che erano simili per il 95% a un embrione di topo naturale della stessa età. “Abbiamo scoperto che queste cellule hanno questa incredibile capacità di auto-organizzazione che può essere liberata se date le giuste impostazioni artificiali”, ha detto Hanna. Tuttavia, il lavoro ha alcune limitazioni importanti. Il giorno 8.5 è ancora relativamente presto; il tempo di gestazione completo per un topo è di 20 giorni. E gli embrioni sopravvissuti così a lungo erano una rarità. Solo circa 50 su 10.000 ammassi cellulari si sono auto-organizzati in embrioni. Il resto non si è sviluppato correttamente.
“Questo è solo un passo, ma un passo molto importante per noi per poter studiare lo sviluppo iniziale”, ha affermato Tesar. “Stiamo attraversando il regno della capacità di generare un embrione da zero e potenzialmente un organismo vivente. È stato un passaggio davvero notevole per il campo”. Mentre gli scienziati sono diventati molto bravi a riavvolgere le cellule mature allo stato più primitivo di cellule staminali, capire esattamente quali segnali chimici faranno sì che una cellula staminale produca i precursori di un fegato o di un rene è stato molto più difficile. Gli esperimenti che tentavano di spingere le cellule staminali a formare tessuti specializzati tendevano invece a produrre miscele di cellule confuse, prive di organizzazione e con la composizione sbagliata dei tipi cellulari.
I ricercatori ritengono che il nuovo lavoro del team di Hanna possa fornire una via da seguire per ottenere quelle ricette corrette, in parte perché il bioreattore trasparente consente agli scienziati di osservare lo sviluppo degli organi davanti ai loro occhi, ma sempre nel contesto dei tessuti di supporto circostanti. E poiché partendo dalle cellule staminali anziché dagli ovuli fecondati, possono produrre queste strutture embrionali in un modo molto più scalabile e controllato. “Questo perfezionerà enormemente la tabella di marcia per la formazione di tessuti e organi”, ha affermato Nicolas Rivron, biologo di cellule staminali presso l’Istituto di biotecnologia molecolare dell’Accademia delle scienze di Vienna. “Ci insegnerà le strutture minime, gli elementi minimi che saranno necessari per formare alla fine organi a tutti gli effetti. Questo da solo non ha prezzo”. Al di là della ricerca di base, tuttavia, l’impatto maggiore di questo lavoro è il suo potenziale per essere applicato un giorno ad altre specie, compreso l’uomo. Gli embrioni sintetici derivati dalle cellule staminali offrono agli scienziati l’opportunità di sondare con dettagli senza precedenti i primi giorni dello sviluppo umano, fornendo al contempo un’alternativa meno controversa ed eticamente irta agli embrioni umani, il cui studio è stato storicamente limitato dai divieti di finanziamento e dalla volontà della fecondazione in vitro donatori:
Occorre ricordare che gli esseri umani hanno periodi di gestazione molto più lunghi e crescono molto più grandi di un topo, oltre ad essere un organismo più complicato. Ma quel tipo di lavoro inizia sempre da qualche parte, e di solito inizia con i topi. Ciò significa che non è troppo presto per iniziare a pensare a dove tutto questo potrebbe essere diretto. “Più dimostriamo sempre più la capacità di spingere gli embrioni derivati da cellule staminali sempre più in via di sviluppo, più gli embrioni sintetici e gli embrioni naturali iniziano a fondersi“, ha affermato Tesar. “Ci sarà sempre un’area grigia, ma come scienziati e come società dobbiamo unirci per decidere dove si trova la linea e definire ciò che è eticamente accettabile“. Hanna, da parte sua, non è interessata agli embrioni sintetici a scopo riproduttivo. L’obiettivo finale a cui sta lavorando è creare organi e tessuti per i trapianti e per curare le malattie umane. Vede gli organoidi sintetici non come potenziali forme di vita quanto la migliore stampante 3D della biologia. “Possiamo interpretarlo come un protocollo di differenziazione universale”, ha detto. Piuttosto che aver bisogno di diverse complicate ricette chimiche per far diventare una cellula staminale un fegato o un polmone, gli embrioni, anche quelli in fase iniziale, possono dare a una cellula staminale tutti i segnali di cui ha bisogno per produrre terapie potenzialmente salvavita. Immagina un paziente con leucemia incurabile:
ha bisogno di un trapianto di midollo osseo per sopravvivere. Nel futuro di Hanna, gli scienziati possono prelevare una biopsia delle cellule della pelle da quel paziente, riavvolgerle in cellule staminali, farle crescere in condizioni ingenue e inserirle in questo bioreattore specializzato. Il risultato finale? Un esercito di cellule staminali del midollo osseo che possono essere somministrate a quel paziente, senza che debbano aspettare una corrispondenza del donatore che potrebbe non arrivare mai. “Siamo agli inizi, ma stiamo davvero aprendo il campo per esplorare queste possibilità in modo più serio”, ha affermato Hanna. “Stiamo passando dalla fantascienza alla scienza”. Video: